Синтез новых производных
дифенилкарбазида на основе a-хлор-алкоксиметил
эфиров и хлоразона и их исследование
Байрамов
Гияс Ильяс оглы,
Бакинский государственный университет.
На основании α-хлор-алкоксиметил
эфиров и хлоразона были синтезированы 8 новых производных дифенилкарбазида,
ранее неизвестных в литературе. Проведено их исследование в качестве
ингибиторов защиты от коррозии металлов в созданных сильно коррозионных средах.
Было установлено, что эти новые соединения (особенно соединения содержащие несколько
функциональных групп и 10 атомов азота) даже при концентрации 2,5; 5; 10 мг/л
обладают свойствами высокоэффективных ингибиторов.
Во
время синтезирования ранее нами новых производных соединений дифенилкарбазида и
дифенилкарбазона и определения их ингибиторной способности, на основании
полученных данных [1–3] можно утверждать, что органические соединения,
содержащие несколько функциональных групп и много атомов азота могут
использоваться как экологически так и экономически высокоэффективные ингибиторы
защиты от коррозии металлов. В связи с этим был проведен синтез новых
производных дифенилкарбазида на основе α - хлор – метил алкил и алкенил
эфиров и хлоразона и получены 8 новых, ранее неизвестных в литературе,
органических соединений, содержащих 10 атомов азота.
Основываясь
на известные методы в литературе [4–8] был проведен синтез новых органических соединений,
условно названных нами соединениями I–VIII. Процентный выход, физико-химические
константы и показатели элементного анализа синтезированных новых органических
соединений I-VIII приведены в табл. 1.
Таблица 1.
Процентный выход, физико-химические
константы и элементный анализ синтезированных новых производных дифенилкарбазида (cоединения I–VIII).
|
Химическая формула соединения и условный номер |
Выход, % |
Ткип, 0С
(мм рт.ст) |
|
|
MRD |
|
Элементный анализ, % Вычислено/ Найдено |
||||
|
Найдено |
Брутто-формула, мол. вес |
C |
H |
N |
Cl |
||||||
|
Вычислено |
|||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
|
|
I |
96.75 |
183-184 (2) |
1.0065 |
1.5213 |
159.21 159.01 |
C31H50O3N4 526 |
70.72 70.57 |
9.51 9.33 |
10.65 10.46 |
– |
|
|
II |
96.84 |
189-190 (2) |
1.0168 |
1.5335 |
177.78 177.60 |
C35H58O3N4 582 |
72.16 71.97 |
9.97 9.79 |
9.62 9.43 |
– |
|
|
III |
96.82 |
195-196 (2) |
1.0267 |
1.5447 |
196.37 196.19 |
C39H66O3N4 638 |
73.35 73.18 |
10.34 10.16 |
8.79 8.58 |
– |
|
|
IV |
95.48 |
217-218 (2) |
1.2120 |
1.5755 |
130.69 130.51 |
C23H28O3N4Cl2 479 |
57.62 57.44 |
5.85 5.69 |
11.69 11.47 |
14,82 14,61 |
|
|
V |
96.68 |
246-247 (2) |
1.1443 |
1.5953 |
266.35 266.17 |
C51H64O5N10 896 |
68.30 68.11 |
7.14 6.96 |
15.63 15.42 |
– |
|
|
VI |
96.59 |
254-255 (2) |
1.1529 |
1.6065 |
285.12 284.94 |
C55H72O5N10 952 |
69.33 69.15 |
7.56 7.37 |
14.71 14.53 |
– |
|
|
VII |
96.64 |
266-267 (2) |
1.1631 |
1.6177 |
303.72 303.53 |
C59H80O5N10 1008 |
70.24 70.03 |
7.94 7.76 |
13.89 13.77 |
– |
|
|
VIII |
95.52 |
289-290 (2) |
1.3131 |
1.6499 |
235.80 235.61 |
C46H42O5N10Cl2 849 |
65.02 64.84 |
4.95 4.76 |
16.49 16.31 |
8.36 8.17 |
|
Где
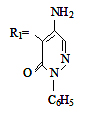
Синтез
соединений I–VIII был проведен нижеследующими этапами:
I. На первом этапе известными способами в литературе [4–7]
были получены α-хлор-метил алкил и алкенил эфиры:
![]()
где R= – C8H17; –C10H21; –C12H25;
–CH2–CH=CCl–CH3.
Структуры,
составы, физико-химические константы и элементные анализы были определены известными
методами. Полученные данные соответствовали показателям известным в литературе
[4–7].
II. На втором этапе была проведена реакция α-хлор-метил-алкил
и -алкенил эфиров с дифенилкарбазидом по известным методам в литературе [8–9]:
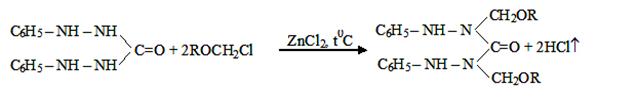
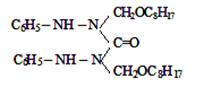
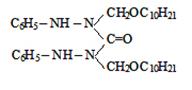
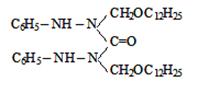
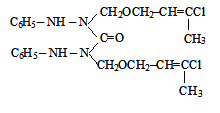
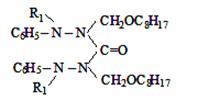
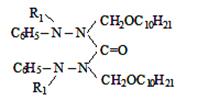
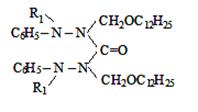
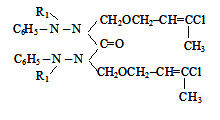
где R= –C8H17(I); –C10H21(II);
–C12H25 (III); –CH2–CH=CCl–CH3
(IV).
III. На третьем этапе была проведена реакция N2,N4-диалкоксиметил- -N1,N5-дифенилкарбазидов (соед. I–IV) с хлоразоном:
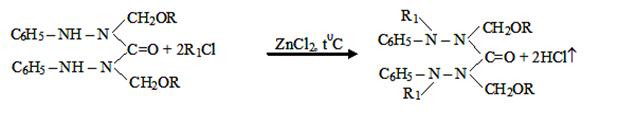
где
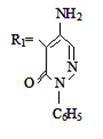
R= –C8H17(V); –C10H21(VI);
–C12H25 (VII); –CH2–CH=CCl–CH3 (VIII).
Во
время исследовательских работ по определению ингибиторной активности новых соединений
I–VIII было установлено, что каждое из них по своей ингибиторной
эффективности превосходит как взятый в качестве сырья для синтеза
дифенилкарбазид, так и многие известные в литературе ингибиторные вещества.
Исследовательские работы по определению ингибиторной эффективности новых
производных дифенилкарбазида (соединения I–VIII) были проведены на основе
известного в литературе [10] «гравиметрического» метода потери массы металла.
Установление эффективности синтезированных
новых производных дифенилкарбазида (I–VIII) в качестве ингибитора коррозии
стали проведено в четырехгорлых колбах в динамических условиях при постоянном
перемешивании (600 об/мин.) коррозионной двухфазной смеси при 40 – 450С.
Образцы из стали 3 с общей поверхностью 2 см2 перед испытанием
шлифуются, обезжириваются соответствующим образом. Расход ингибитора
рассчитывается на
Таблица 2.
Показатели результатов исследования
ингибиторной эффективности
новых производных дифенилкарбазида (соединения I – VIII).
|
Условный номер соединения |
Концентрация ингибитора, мг/л |
3% NaCl+нефт (10:1) H2S 500 мг/л |
0.3 N HCl +бензин (1:7) H2S 1000 мг/л |
||
|
Скорость коррозии, г/см2 час |
Эффективность ингибитора, % |
Скорость коррозии, г/см2 час |
Эффективность ингибитора, % |
||
|
1 |
2 |
3 |
4 |
5 |
5 |
|
Без ингибитора |
– |
2.56 |
– |
3.65 |
– |
|
I |
2.5 5 10 |
0.184 0.096 0.049 |
92,81 96.25 98.09 |
0.362 0.175 0.081 |
90.08 95. 21 97.78 |
|
II |
2.5 5 10 |
0.161 0.082 0.038 |
93.71 96.79 98.52 |
0.340 0.152 0.067 |
90.68 95.84 98.16 |
|
III |
2.5 5 10 |
0.138 0.070 0.027 |
94.61 97.27 98.95 |
0.318 0,135 0.051 |
91.29 96,30 98.60 |
|
IV |
2.5 5 10 |
0. 081 0.023 0.011 |
96.84 99.10 99.76 |
0.098 0.0126 0.0005 |
97.32 99.65 99.98 |
|
V |
2.5 5 10 |
0.0008 0.0002 - |
99.97 99.99 100 |
0.0002 0.0001 - |
99.99 100 |
|
VI |
2.5 5 10 |
0.0002 0.0001 |
99.99 100 |
0.0002 - |
99.99 |
|
VII |
2.5 5 10 |
0.0001 |
100 |
0.0001 |
100 |
|
VIII |
2.5 5 10 |
- |
100 |
- |
100 |
|
А [11] |
200 |
0.038 |
98.5 |
0.073 |
98 |
Как
видно из табл. 2, даже при концентрации 2.5; 5; 10 мг/л полученные нами новые соединения
I–VIII (особенно соединения V–VIII) по своим ингибиторным свойствам
превышают взятое нами для сравнения известное в литературе [11] условно
обозначенное нами А, ингибиторное вещество, получившее авторское свидетельство,
даже при его концентрации 200 мг/л.
Исследования
показали, что на эффект защиты оказывает влияние не только наличие или отсутствие
кратной связи, а так же природа и количество функциональных групп и количество
атомов азота. Все это способствует образованию комплекса между молекулой
ингибитора и металлом и приводит к повышению степени защиты.
А так
же вероятнее всего, что новые синтезированные соединения I– VIII
адсорбируются на поверхности стали и, проявляя свою ингибиторную
активность, положительно действуют на сталь, делая ее поверхность пассивной для
коррозии. За счет наличия в составе новых соединений двойных связей, функциональных
групп, атомов азота и за счет повышения плотности электронов в их составе поверхность
стали становится пассивной к коррозии.
На
основании исследовательской работы можно заявить, что синтезированные новые
производные дифенилкарбазида (соединения I–VIII, а особенно соединения V– VIII) могут
использоваться как высоко-эффективные ингибиторы защиты от коррозии стального
технологического оборудования в нефтегазодобывающей, перерабатывающей промышленности,
а так же и в нефтехимической промышленности.
Как
видно из строения и состава соединений I– VIII можно вести исследования для использования
их в разных направлениях, поэтому очень актуален синтез таких соединений в
нефтехимической промышленности, а так же в промышленности органической химии.
Экспериментальная
часть
Синтез N2,N4-диоктоксиметил-N1,N5 -дифенилкарбазида
(1). В
реакционную колбу помещают
Синтезированный
N2,N4-диоктоксиметил-N1,N5-дифенилкарбазид (I) от-гоняется на вакуумной установке.
Аналогично
синтезу соединения I был проведен синтез
N2,N4-дидeсоксиметил-N1,N5-дифенилкарбазида (II), N2,N4-диундесоксиметил-N1,N5- -дифенилкарбазида (III) и N2,N4-ди(2-хлор-5-оксогексен-2)-N1,N5-дифенил-карбазида (IV).
Составы
и структуры синтезированных новых соединений были установлены на основании
данных элементного анализа, ИК и масс спектров.
В ИК
спектре этих соединений интенсивно проявляются полосы характеризующие простую
эфирную группу С-О-С 1050, 1080 см-1; связь С-N 1310, 1350 см-1;
СН3 группу 1380, 1460, 2990,3030 см-1; СН2
группу 2950 см-1; NH-N группу 1580 см-1, NH группу 3400,
3450 см-1; содержащуюся в ядре бензола С=С связь 1440–1465, 1500–1510,
1590–1610 см-1; С6Н5 группу 700–780 см-1.
В ИК-спектре
соед. IV наряду с перечисленными выше харак-теристиками структуры
интенсивно проявляются полосы, относящиеся к 2 – хлор-5-оксогексен-2 группе
связь С=С 1640 см-1; С-Сl связь 650 см-1.
В масс
спектрах соединений I-IV было определено, что их молекулярным массам соответствуют
молекулярные ионы 526 m/е, 582 m/е и 638 m/е и 479 m/е.
Синтез N1,N5-диазон-N2,N4-диоктоксиметил-N1,N5-дифенилкарбази-да
(V). В реакционную колбу для синтеза помещают
Синтез соединений N1,N5-диазон-N2,N4-дидесоксиметил-N1,N5-дифенил-карбaзида (VI), N1,N5-диазон-N2,N4-диундесоксиметил-N1,N5-дифенилкарбa-зида (VII) и N1,N5-диазон-N2,N4-ди(2-хлоp-5-оксогексен-2)-N1,N5-дифенил-карбазида (VIII) был
проведен аналогично синтезу соединения V.
Составы
и структуры синтезированных новых соединений дифенилкарбазида V–VIII были
установлены на основании данных элементного анализа, масс и ИК-спектров.
В ИК-спектре
этих соединений интенсивно проявляются полосы характеризующие простую эфирную
группу С–О–С 1050, 1080 см-1; СН3-груп-пу 1380, 1460,
2990 см-1; СН2-группу 2950 см-1; связь С-N
1310-1350 см-1; N–N-группу 1580 см-1, в группе азона NH2-группу
550, 1570, 3300 см-1; содержащуюся в ядре бензола С=С связь 1440 , 1465, 1500 –
1510, 1590 – 1610 см-1; С6Н5 группу 700 – 780
см-1.
В ИК
спектре соед. V–VIII наряду с перечисленными выше характеристиками структуры
интенсивно проявляются полосы, относящиеся к 2-хлор-5-оксогексен-2 группе связь
С=С 1640 см-1; С–Сl связь 650 см-1.
В масс
спектрах соединений V–VIII было определено, что их молекулярным массам соответствуют
молекулярные ионы 896 m/е, 952 m/е и 1008 m/е и 851 m/е.
Литература
1.
Байрамов Г.И. Синтез серо-, а так же азот-и серосодержащих новых
органических соединений на основе 1-метил-1-хлор-2-октоксиметилциклогек-сана.
// Химические проблемы. НАН Азербайджана. 2008.№ 1. с.96.
2.
Байрамов Г.И. Синтез и исследование азотсодержащих новых
органических соединений на основе 1,3-дихлорбутена-2. // Азерб. хим. журн.,
2008. № 2. с.102.
3.
рачев Х., Стефанова С. Справочник по коррозии. М.: Мир,
1982. С.62.
4.
Исагулянц В.И. и др. 1,3-дихлорбутен-2 и новые препараты на его
основе. //Журн. Успехи химии, 1964. т.XXXIII,
вып.I, С.55.
5.
Поконова Ю.В. химия
и технология галоген эфиров – Л.: ЛГУ. 1982. с.243.
6.
Поконова Ю.В Галлоиды эфиров. М.: Химия. 1966. С.57.
7.
Байрамов Г.И. Дисс. …канд.хим.наук. Баку: ИНХП АН Азерб. ССР,
1988. с.80, 82.
8.
Байрамов Г.И. Синтез и исследование новых азотсодержащих
органических соединений на основе эфиров α-хлор-алкоксиметила.
//Химические проблемы. НАН Азербайджана. 2008. № 4. с.628.
9.
Байрамов Г.И. Синтез новых азотсодержащих органических соединений
на основе 2,6-дихлор-5-оксогексен-2 эфира и их исследование. //Азерб. хим.
журн., 2008. № 3. с.179.
10.
Жук Н.П. Курс коррозии и
защита металлов. М.: Металлургия, 1968. С.361.
11.
Шихмамедбекова А.З, мамедьярова И.Ф, Байрамов Г.И и др.
«N,N'-дифенил-N'-октоксиметил-гуанидин в качестве
ингибитора коррозии стали в двухфазной системе». Автор. Свид. СССР. №1031141,
Поступила в редакцию 09.04.2009 г.