Разработка нелинейной
математической модели процесса сжигания твёрдого топлива
Косенко Максим Вячеславович,
аспирант
Московского энергетического института,
Кромов Иван Сергеевич,
соискатель
Ивановского государственного энергетического университета,
инженер по
наладке и испытаниям оборудования ОАО «Ивэлектроналадка».
В
статье рассматриваются основы математического моделирования топочных процессов
котельных агрегатов, рассчитанных на сжигание твёрдого топлива и газа. Приведены
основные уравнения и допущения, применяемые при моделировании. Разработана
математическая модель процесса сжигания твёрдого топлива, описанная системой
нелинейных дифференциальных уравнений, включающей уравнения неравновесной
термодинамики, которая может быть положена в основу автоматических систем
регулирования тепловой нагрузки в котлах.
| Https://energomir.su/kotli-otopleniya/tverdotoplivnie https://energomir.su/kotli-otopleniya/tverdotoplivnie - твердотопливные котлы energomir.su |
Задачей представленной работы
являлась разработка динамической нелинейной математической модели процесса
сжигания твёрдого топлива, отражающей реальные физико-химические процессы, протекающие
при горении. В настоящее время на решение проблемы создания высокоточных
математических моделей энергоблоков направлены усилия многих специалистов. Однако
процессы сжигания топлива в топочных камерах котлов на протяжении длительного
времени остаются слабым звеном при построении моделей энергоблоков. Поэтому
поставленная в работе задача представляется своевременной и актуальной.
За
основу процесса моделирования первоначально были положены известные математические
описания физико-химических процессов горения твёрдого топлива в топочных камерах
котлов в статическом режиме, наиболее полно представленные в работах профессора
В.В.Померанцева и его учеников [1]. За основу динамических особенностей
процессов горения топлива были взяты результаты работы В.В.Крашенинникова, П.Профоса
и В.И.Бабия [2]. Инновационным же в
рассмотренном подходе является использование метода феноменологической термодинамики,
разработанного профессором Н.Н.Семёновым [3].
Обобщёно, процесс горения
твёрдого топлива протекает при наличии следующих физико-химических процессов:
-
движение в топочной камере подаваемых в неё компонентов горючей смеси;
-
наличие турбулентной и молекулярной диффузии исходных веществ и продуктов
реакции;
- теплообмен в газовых потоках продуктов
сгорания и исходной смеси;
- конвективный и радиационный теплообмен
горящих частиц с газовой средой;
- процессы нагрева частиц, возгонки летучих,
переноса и горения их в газовом объёме.
В
связи со сложностью протекающих аэродинамических и физико-химических процессов,
и их значительной зависимости от трёх пространственных координат, при создании
математической модели был принят ряд допущений, а именно предполагается, что:
- реагирование протекает на поверхности
углеродных частиц сферической формы одинаковых размеров;
- горение выделяющихся летучих веществ и
догорание продуктов неполного сгорания происходит в объёме газовой среды;
- конвективным переносом теплоты из системы и
диффузионной теплопроводностью можно пренебречь.
При
принятых допущениях метод феноменологического описания в данной работе
заключается в том, что для описания топочных процессов горения твёрдого топлива
были составлены законы сохранения массы, энергии и количества движения,
являющиеся следствиями первого и второго законов термодинамики. При этом при
протекании в топочной камере химических реакций и фазовых переходов в правые
части уравнений законов сохранения массы для компонентов реагирующей смеси были
включены удельные мощности изменения масс компонентов.
В
результате общая система уравнений законов сохранения, описывающая топочные
процессы, имеет вид:
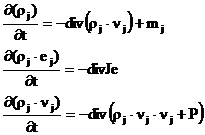
![]() (1)
(1)
где ρi – плотность потока переносимой массы i-го компонента в элементарном объёме;
νi – скорость центра масс элементарного объёма,
м/c;
e – полная энергия на единицу массы i-го компонента, Дж/кг;
Je – полный удельно-массовый поток энергии,
Вт/м2;
P – тензор давлений на элементарный объём, Па;
mj – удельная мощность изменения массы j-го компонента, (кг/с)/м3.
Решение этой системы уравнений в
общем виде не представляется возможным, поэтому был осуществлён переход к
одномерной модели, а затем к модели с сосредоточенными параметрами.
При этом система уравнений (1)
принимает следующий вид:
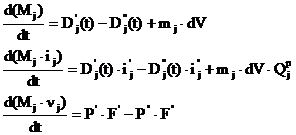 (2)
(2)
где Dj’ и Dj’’– расход j-го
компонента смеси на входе и на выходе моделируемой системы;
Mj – масса j-го компонента в объёме системы;
dV – объём моделируемой элементарной области;
ij’ и ij’’– энтальпия j-го
компонента смеси на входе и на выходе моделируемой системы;
Qjp – теплота сгорания j-го компонента.
На примере рассмотрения горения
угольной частицы комплекс (mj·dV) для углерода частицы
был выражен через скорость выгорания углерода, которая в свою очередь была
найдена при допущении, что изменение констант скоростей реакций от температуры подчиняется
закону Аррениуса:
![]() (3)
(3)
![]() (4)
(4)
где Gc – скорость горения углерода, кмоль/(м2·с);
MмолС = 12 ![]() - молекулярная
масса углерода;
- молекулярная
масса углерода;
Fпов. – площадь поверхности реагирующих частиц;
kc – константа скорости горения углерода.
Имеется обширнейший
экспериментальный материал по определению кинетических констант реакции горения
углерода, но следует отметить, что эти данные, полученные с применением
различных экспериментальных методик на разных видах углеродного материала,
отличаются большим разнообразием. В данной работе для уравнения (4) константа
скорости химической реакции горения углерода (С + О2 ↔ СО2)
была выражена через энергию активации реакции Ес при предположении о
наличии некоторой условной точки – полюса, в которой сходятся линии констант
скорости реакций:
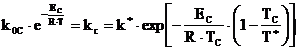 (5)
(5)
где {k*; T*}
= {10 м/c; 2500 К} – координаты полюса
согласно [3].
Аналогичным образом, согласно
(3)-(5), были выражены скорости расхода кислорода, скорости образования СО2
и при необходимости (наличие восстановительной среды) угарного газа СО.
Для применения выражения (3)
традиционно сложным и до конца не исследованным вопросом является определение
площади поверхности реагирующих частиц. Данный вопрос наиболее полно рассматривался
в работах Г.Т.Левита и С.Н.Миронова [4]. При разработке математической модели в
рассматриваемой работе площадь пыли определялась из зерновой характеристики
топлива по методике Г.Т.Левита, основанной на использовании формулы Розина – Рамлера
– Беннета (РРБ). Дополнительно была введена поправка на реальную форму частиц
угольной пыли, отличающуюся от сферической.
Дополнительно
был выполнен расчёт концентраций оксидов азота (NOx) в уходящих дымовых газах. Расчёт
концентраций NOx произведён на основе теории Семёнова-Зельдовича-Франк-Каменецкого при
рассмотрении совокупности цепных реакций с участием атомарного кислорода и
азота:
О + N2
![]() NO + N (6)
NO + N (6)
N + O2 ![]() NO + O (7)
NO + O (7)
где
k1-k4 – скорости
протекания прямых и обратных реакций (6) и (7).
Кинетика реакций (6-7) определяется уравнениями [5]:
![]() (8)
(8)
![]() (9)
(9)
В расчете принималось допущение, что скорость изменения концентрации
атомарного кислорода и азота намного меньше, чем скорость изменения
концентрации оксида азота, т.е. ![]() , в результате:
, в результате:
![]() (10)
(10)
В свою
очередь выражение (8) после ряда преобразований было сведено к виду:
![]() (11)
(11)
где С(NO) – равновесная концентрация оксида азота;
K0 – константа равновесия реакции диссоциации
молекулы кислорода.
Константа
равновесия цепных реакций образования NO:
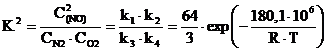 (12)
(12)
Согласно [ 5]
для комплекса (K0·k1) принимается:
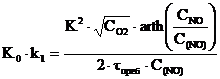 (13)
(13)
где τпреб
– время пребывания частиц в рассчитываемой зоне топочной камеры.
Аналогичным
образом был произведён учёт частичного восстановления оксидов азота в зонах с недостатком
окислителя, которыми являются зона горения коксового остатка (α ≈
0,95-1,0). Динамика процесса восстановления NOx в указанной зоне обусловлена динамикой протекания реакции:
2NО + 2CO ![]() N2 + 2CO2 (14)
N2 + 2CO2 (14)
Пренебрегая
скоростью протекания обратной реакции, для реакции восстановления (14) справедливо:
![]() (15)
(15)
Путём
сопоставления уравнений (11) и (15) была определена доля оксида азота, восстанавливаемого
до молекулярного азота N2 в зонах с недостатком окислителя. При этом
константы скоростей реакций k1 и k5 были выражены через энергии активации приведённых реакций E1 и E5 согласно введению полюса В.В.Померанцева.
Энергия активации цепной реакции образования оксидов азота (E1 = 180 кДж/моль) была рассчитана и в дальнейшем многократно уточнена
академиком Я.Б.Зельдовичем [5]. В свою очередь, энергия активации реакции
восстановления оксида азота (Е5) была рассчитана по приближённой
методике Н.Н.Семёнова [3] для случая экзотермической реакции:
Е5
= Е0 ≈ 11,5 – 0,25Q ![]() (16)
(16)
где
Е0 – высота потенциального активационного барьера реакции восстановления;
Q
– теплота реакции восстановления NO.
В результате общая система
уравнений, описывающая топочные процессы сжигания твёрдого топлива, приведена к
виду:
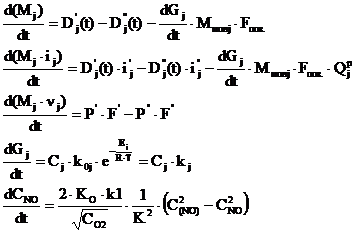 (17)
(17)
Полученная система отличается
тем, что:
1) в правые части уравнений
законов сохранения массы для компонентов реагирующей смеси были включены удельные
мощности изменения масс компонентов mj;
2) система уравнений дополнена
уравнением скорости горения компонентов исходной смеси Gj, необходимым для расчета мощности изменения
массы;
3) дополнительно включено
уравнение для расчёта концентраций оксидов азота в продуктах сгорания
рассчитываемой зоны.
На
основе полученной системы дифференциальных уравнений, описывающих нелинейную
математическую модель процесса сжигания топлива, была реализована имитационная
модель топочной камеры котла в системе имитационного моделирования VisSim. Полученные результаты являются основой для
синтеза автоматических систем регулирования в составе полномасштабных АСУТП
энергоблоков тепловых электростанций, сжигающих твёрдое и газовое топливо.
Литература
1. Основы практической теории горения: учеб. пособие для вузов / под ред. В. В. Померанцева. – 2-е изд., перераб. и доп. – Л.: Энергоатомиздат. Ленингр. отд-ние, 1986. – 312 с.: ил.
2. Бабий, В. И. Горение угольной пыли и расчёт пылеугольного факела / В. И. Бабий, Ю. Ф. Куваев. – М.: Энергоатомиздат, 1986. – 208 с.
3. Семёнов, Н. Н. О некоторых проблемах химической кинетики и реакционной способности / Н. Н. Семёнов. – М.: Изд-во АН СССР, 1958. – 686 с.
4. Левит, Г. Т. Пылеприготовление на тепловых электростанциях / Г. Т. Левит. – М.: Энергоатомиздат, 1991. - 384 с.
5. Зельдович, Я. Б. Физика ударных волн и высокотемпературных гидродинамических явлений / Я. Б. Зельдович, Ю. П. Райзер. – 2-е изд., перераб. и доп. - М.: Наука, 1976. – 686 с.
Поступила в редакцию 09.12.2009 г.