Маркеры различия тяжелой
БА и ХОБЛ с необратимой бронхиальной обструкцией: фокус на клеточный состав и
цитокиновый спектр индуцированной мокроты
Садыгов Ализаман Сиясет оглы,
доктор медицинских наук,
Исмаилзаде Дж.М.
Кафедра легочных
заболеваний Азербайджанского медицинского университета.
Хроническая
обструктивная болезнь легких (ХОБЛ) и бронхиальная астма (БА) – два самостоятельных
хронических заболевания респираторной системы, наиболее распространенные среди
населения [1]. Несмотря на вполне определенные различия между ХОБЛ и БА по
механизмам развития, клиническим проявлениям и принципам профилактики и
лечения, эти заболевания имеют некоторые общие черты. Кроме того, возможно
сочетание их у одного человека. Все это создает известные трудности в практической
работе даже хорошо информированного врача [2].
Дифференциальная диагностика БА и ХОБЛ основана
на интеграции основных клинических результатов функциональных и лабораторных
тестов. Однако в случае тяжелой и резистентной терапии БА диагностическая значимость
бронходилатационного теста в отношении дифференциации астмы от ХОБЛ значительно
снижается [3]. В настоящее время еще нет лабораторного маркера надежно
дифференцирующего эти две болезни [4].
Целью настоящего
исследования явилось изучение клеточного состава и цитокинового спектра мокроты
и возможность применения этих показателей для дифференциации тяжелой БА и ХОБЛ
с необратимой бронхиальной обструкцией.
Материалы
и методы
В период с апреля
Результаты
Из
64 отобранных больных с необратимой бронхиальной обструкцией в исследовании приняло
участие 43. Пациенты с тяжелой БА (n=19) и ХОБЛ II и III стадией (n=24) значимо не различались по возрасту
(62,2 и 62,8 года соответственно), полу и длительности заболевания (табл. 1).
Таблица 1.
Исходная
характеристика больных, включенных в исследование.
|
Показатели |
Тяжелая БА |
ХОБЛ II-III стадии |
|
Число больных |
19 |
24 |
|
Пол: м/ж |
12/7 |
18/6 |
|
Средний возраст, лет |
62,2 (35-75) |
62,8 (40-70) |
|
Длительность заболевания |
9,8±2,86 |
9,2±1,75 |
|
ОФВ₁/ФЖЕЛ, % |
67,2±5,46 |
64,6±3,51 |
|
ОФВ₁, % от должн. |
57,3±11,46 |
56,4±12,34 |
|
Общий IgE, МЕ/мл |
296,4±18,46* |
48,6±5,37 |
* -
р<0,05 при сравнении между группами.
Отмечено, что среди
лиц с БА не было курильщиков, а в семейном анамнезе регистрировались случаи БА
и другие проявления аллергии. В то же время все больные ХОБЛ курили, стаж
курения превышал 24 пачка-лет, в анамнезе, в том числе семейном, не фигурировали
БА и другие аллергические заболевания. Пациенты с БА отличались от больных
ХОБЛ по уровню IgЕ
в сыворотке крови (296 vs
48 МЕ/мл) и количеству позитивных накожных тестов (53,9 vs 8,2%). Степень
бронхиальной обструкции у больных ХОБЛ и тяжелой БА была одинаково выражена
(ОФВ₁ 56,4 и 57,3% от должного) в то время как
обратимость бронхообструкции после 14-дневного курса ГКС была больше выражена
среди лиц с тяжелой БА. У больных ХОБЛ и БА различались также и парциальное
давление кислорода артериальной крови (PaO₂) и насыщение
крови кислородом (SaO₂)
(81,4 vs
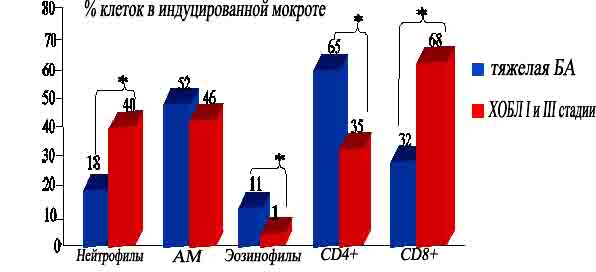
Рис. 1. Морфологические
особенности воспаления дыхательных путей у больных тяжелой БА и ХОБЛ II-III стадии. * - р<0,05 при сравнении между группами.
Содержания
субпопуляций Т-лимфоцитов (СD4+
и СD8+)в
индуцированной мокроте достоверно отличалось. Для больных с тяжелой БА характерно
значительное повышение содержания СD4+ Т-лимфоцитов в сравнении с больными ХОБЛ II
и III стадий (65% vs 35%). Напротив, у больных ХОБЛ было отмечено значительно
содержание СD8+
Т-лимфоцитовв (68 vs 32%).
Данные, полученные в
ходе исследования, показали, что при сравнении больных тяжелой БА и ХОБЛ с II
и III стадией отмечается достоверное различие уровня IL-4 и IL-8. У больных с тяжелой БА выявлено более
высокое содержание IL-4
в индуцированной мокроте в сравнении с пациентами ХОБЛ II-III стадии (31,8 vs
3,1 пг/мл, р<0,01). У пациентов с ХОБЛ в сравнении с больными тяжелой БА
было зафиксирована значительное увеличение содержания IL-8 в индуцированной мокроте (32,7 vs 10,4
пг/мл, р<0,01). Содержания IL-6
и TNF-α в индуцированной мокроте у больных обеих
групп существенно не различались (табл. 2).
Таблица 2.
Содержание
цитокинов в индуцированной мокроте у больных тяжелой БА и ХОБЛ (M ±
m).
|
Показатели (пг/мл) |
Тяжелая БА |
Больные ХОБЛ II-III стадии |
|
TNF – α |
21,8±1,69 |
26,9±1,55 |
|
IL – 4 |
31,7±2,18* |
3,1±0,84 |
|
IL – 6 |
20,4±1,83 |
25,6±2,41 |
|
IL – 8 |
10,4±1,76 |
32,7±2,19* |
* -
р<0,05 при сравнении между группами
Таким образом, у людей
с необратимой бронхиальной обструкцией характер воспаления в дыхательных путях
различается при тяжелой БА и ХОБЛ II-III стадии, а сам факт необратимости не
позволяет исключить БА у таких пациентов.
Заключение.
Следует отметить, что
большой интерес понимания патогенеза тяжелой БА и ХОБЛ и особенностей иммунной
системы при этих заболеваниях представляет рассмотрение цитологического состава
и спектра интерлейкинов индуцированной мокроты. Исследования показали, что
измерения легочных объемов, обратимости вентиляционных нарушений на ГКС не
являются ключевыми методами в проведении дифференциального диагноза между двумя
обструктивными заболеваниями. Напротив, такие неинвазивные методики, как
определение содержания эозинофилов и нейтрофилов, а также про- и противовоспалительных
цитокинов (IL-4
и IL-8)
в индуцированной мокроте, могут помочь выявить тяжелую БА с необратимой бронхиальной
обструкцией. Суммируя полученные результаты, следует отметить, что при ХОБЛ и
тяжелой БА регистрируется гиперцитокинемия как за счет провоспалительных (IL-6,8 и TNF-α), так и противовоспалительных цитокинов
(IL-4).
Однако характер изменения гиперцитокинемии при ХОБЛ в отличие от больных
тяжелой БА резко отличается. Если у больных с ХОБЛ гиперцитокинемия в индуцированной
мокроте отмечается основном за счет провоспалительных цитокинов, у больных
тяжелой БА геперцитокинемия в индуцированной мокроте обусловлено в основном
за счет противовоспалительных цитокинов.
Литература
1.
Barnes
P.J.,
2.
Bateman
E.D., Boushey H.A., Bousquet J. et al. Can guideline – defined asthma control
be achieved? The Gaining Optimal Asthma Control Study. Am. J. Respir. Crit.
Care Med. 2004; 170 (8): 836-844.
3.
Global
Initiative for Asthma. Global Strategy for asthma management and prevention.
Workshop Report, 2007 htttp://www.ginasthma.com.
4.
Global
Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive
Pulmonary Disease: Updated 2007.
Поступила
в редакцию 07.05.2009 г.