Система саморегуляции легочного дыхания
Васильев Геннадий Федорович,
Работа относится к области биологии и посвящена анализу процесса дыхания человека.
Как известно, дыхание – это процесс снабжения организма кислородом. Кислород необходим организму для использования энергии, синтезированной митохондриями клеток. Процесс дыхания – это сложный процесс, обеспечиваемый работой нескольких скоординированных между собой систем. Система легочного дыхания – одна из них, причем, по процедуре – первая. Т.е. от ее нормального функционирования зависят условия работы всей последующей цепочки.
Главной задачей системы легочного дыхания является доставка кислорода из атмосферного воздуха в кровь и поддержание его концентрации в артериальной крови на необходимом уровне, как в состоянии покоя, так и при физической нагрузке. Таким образом, регулируемой величиной системы (далее, РВ) является концентрация кислорода в артериальной крови или Pao2.
Исполнительным механизмом системы (далее, ИМ) является сложное устройство, состоящее из легких, грудной клетки, множества дыхательных мышц, мотонейронов дыхательных мышц, расположенных в спинном мозге, и дыхательного центра, расположенного в продолговатом мозге. Координирует работу всех частей дыхательный центр. На него подается управляющее воздействие системы.
Функционирование ИМ обеспечивает необходимое значение РВ. При этом он имеет возрастающую статическую характеристику, т. к. при увеличении значения управляющего воздействия происходит увеличение значения РВ.
Формирователем закона управления (далее, ФЗУ) являются хеморецепторы каротидных телец, расположенные в местах разветвления сонной артерии на внутреннюю и внешнюю ветви, чувствительные к снижению концентрации кислорода в артериальной крови. При снижении значения Pao2, увеличивается частота импульсации в синокаротидном нерве. Таким образом, на вход ФЗУ поступает текущее значение РВ, а на выходе возникает соответствующее ей значение сигнала управления (далее, СУ). ФЗУ данной системы имеет убывающую статическую характеристику.
Сигнал управления (импульсация в синокаротидном нерве) поступает на вход исполнительного механизма (в дыхательный центр). Таким образом, возникает замкнутая система с отрицательной обратной связью, способная стабилизироваться при некотором значении концентрации кислорода в артериальной крови, несмотря на возмущающие факторы, главным из которых является изменение потребления кислорода.
Подробнее с методологией системного анализа, адаптированной для биологических объектов (основы регуляции, терминология, характеристики), можно ознакомиться в [1].
На рис. 1 приведена функциональная схема системы саморегуляции легочного дыхания, а на рис. 2, ее рабочая характеристика. Как видно из статической характеристики ФЗУ, она имеет существенную нелинейность. Благодаря этому при малых нагрузках (до 50 Вт), ФЗУ находится в зоне безразличия. В этой зоне значение Pao2 достаточно велико, и сигналы от синокаротидных телец не принуждают дыхательный центр к усилению диффузии кислорода. В этой зоне дыхательный центр реагирует на сигналы хеморецепторов двуокиси углерода, определяя тот или иной паттерн дыхания. Этот режим хорошо исследован и подробно описан в физиологии дыхания. При нахождении ФЗУ в зоне безразличия, возможно также произвольное дыхание (прямое воздействие на дыхательные мотонейроны из двигательной области коры головного мозга).
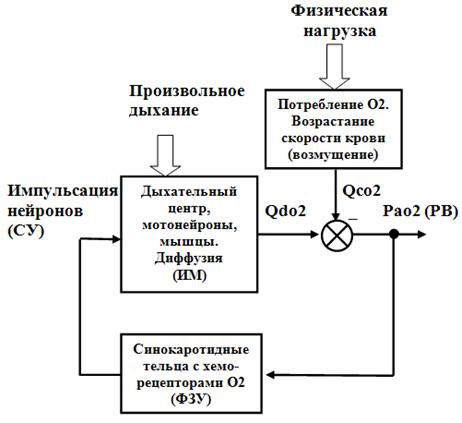
Рис. 1. Функциональная схема системы саморегуляции легочного дыхания: Qdo2 – текущее значение потока диффузии кислорода в кровь легочных капилляров; Qco2 – текущее значение потока потребления кислорода тканями; Pao2 – текущее значение парциального давления кислорода в артериальной крови.
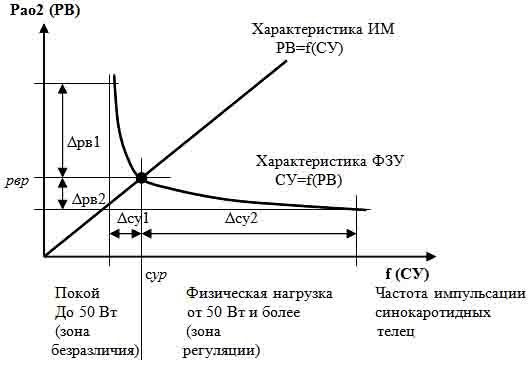
Рис. 2. Рабочая характеристика системы саморегуляции легочного дыхания: рвр – значение РВ в состоянии равновесия системы; сур – значение СУ в состоянии равновесия системы.
При возрастании нагрузки до значения 50 Вт и более ФЗУ начинает активизироваться вследствие снижения Pao2 и, следовательно, возрастания импульсации от синокаротидных телец (зона регуляции). В начале диапазона имеет место некоторая промежуточная зона, когда человек усилием воли еще может внести какие-то произвольные условия в работу дыхательного центра. Но при дальнейшем увеличении нагрузки (и эта величина индивидуальна, см. [4], с. 20, таблица 2) наступает момент, когда режим дыхания, задаваемый дыхательным центром, усилием воли уже не перебороть. Дыхательный центр полностью захватывает инициативу и включает в действие все имеющиеся ресурсы для обеспечения организма кислородом при текущем уровне нагрузки.
На рис. 3 приведена нагрузочная характеристика кардио-респираторной системы, которая показывает, как изменяются регулируемые величины системы, при изменении нагрузки. Эта характеристика построена на основе экспериментальных данных (Doll E. J., Keul J., Maiwald C. et al, 1968), приведенных в [4]. Более подробное описание этого эксперимента и процедура формирования этой характеристики приведены в [2].
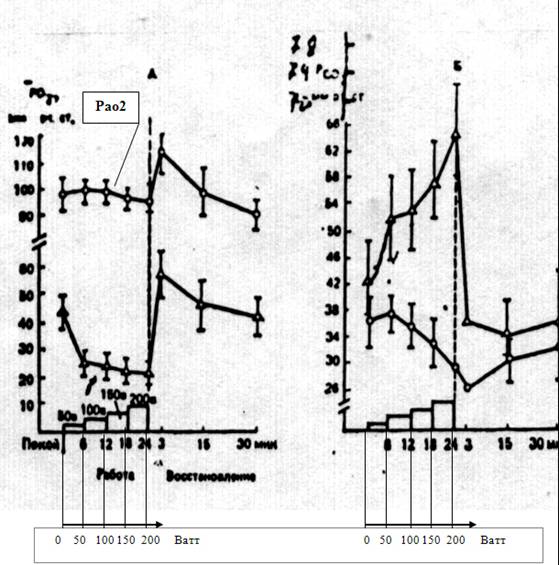
Рис. 3. Нагрузочная характеристика кардио-респираторной системы. Изменения Po2 (А) и Pco2 (Б) в артериальной и венозной крови у испытуемых во время ступенчатой работы на велоэргометре
(В.В.Михайлов. Дыхание спортсмена. Москва, «Физкультура и спорт», 1983 год (E Doll, J Koul, C Maiwald, H. Reindell, 1968)).
Работу системы саморегуляции легочного дыхания описывает кривая Pao2 (см. рис. 3 А, верхняя кривая). Здесь видно, что до значения величины нагрузки 50 Вт ФЗУ не вмешивается в процесс регуляции. Интенсивность вентиляции легких определяется дыхательным центром под воздействием двуокиси углерода. При этом имеет место некоторый рост значения Pao2. Объясняется это следующим образом.
Известно, что диффузия происходит эффективно, если интенсивность вентиляции альвеол соответствует интенсивности их перфузии. Но в покое эффективно используется только средняя часть легких. В верхней части легких уменьшена перфузия, и вентиляция этой части легких не дает нормального эффекта. В нижней части легких усиленная перфузия не обеспечивается должной вентиляцией, что снижает эффективность диффузии. Это увеличивает венозную примесь в артериальной крови, снижая значение Pao2. Таким образом, при малой вентиляции существенная часть ресурсов легких находится в резерве, а Pao2 – несколько снижено.
При возрастании вентиляции, газообмен в нижней части легких становится адекватным величине перфузии. Венозная примесь в артериальной крови уменьшается, и Pao2 начинает подрастать, что и отражается некоторым ростом кривой.
При дальнейшем возрастании нагрузки увеличивается также и перфузия альвеол верхних частей легких, что включает их в работу. По данным [5] (см. с. 591) в покое не работают до 50% легочных капилляров. Включение в работу дополнительных капилляров не только увеличивает поверхность АКМ, но и снижает скорость крови в легочных капиллярах. Это увеличивает время нахождения эритроцитов в легочном капилляре и способствует большему насыщению эритроцитов кислородом, что увеличивает поток диффузии.
Итак, при значении нагрузки 50 Вт и более вступает в действие ФЗУ, и саморегуляция не позволяет значению Pao2 уменьшаться, не смотря на существенное увеличение (до 10 раз при максимальной нагрузке) потребления кислорода (см. [3], с.124, таблица 18). Имеющий место некоторый наклон нагрузочной характеристики Pao2 в диапазоне от 50 до 200 Вт объясняется статической ошибкой системы.
Столь высокую производительность легких в процессе диффузии кислорода при физической нагрузке физиология пока объяснить не может. Объяснение того, какими ресурсами владеет дыхательный центр для обеспечения необходимого потока диффузии из альвеолярного пространства в кровь легочного капилляра предпринято в [2] (см. http://jurnal.org/articles/2014/biol4.html). Поскольку задача объяснения этого явления остается актуальной, исследования продолжаются. Ниже приводятся результаты исследования процесса диффузии в легких, проведенного автором на математической модели.
При разработке модели диффузии кислорода в легких использовано описание процесса, приведенное в [5] (см. с. 589-590). Вентиляция легких в состоянии покоя обеспечивает парциальное давление кислорода в альвеолярном газе равным приблизительно 100 мм рт.ст. На вход легочного капилляра поступает венозная кровь, концентрация кислорода в которой соответствует парциальному давлению равному 40 мм рт.ст. Возникает диффузионный поток кислорода из газа альвеолярного пространства в кровь капилляра. По мере прохождения эритроцитов по капилляру, они все больше насыщаются кислородом, а градиент давлений уменьшается. В конце капилляра напряжение кислорода в крови повышается почти до 100 мм рт.ст., а градиент давлений уменьшается до нуля. Диффузия кислорода в отдельно взятый эритроцит прекращается. Время прохождения эритроцита по легочному капилляру составляет, 0,3 сек.
Таким образом, процесс диффузии кислорода из альвеолы в кровь капилляра в состоянии покоя иллюстрируется экспоненциальной кривой ([5] см. рис. 21.23, с. 590) с постоянной времени приблизительно 0,1 сек, асимптотой которой является уровень парциального давления кислорода в альвеолярном пространстве PAo2, равный 100 мм рт.ст. Такая экспонента может быть описана выражением:
Po2 = PAo2*(1 – E^-t/T),
где: Po2 – текущее значение напряжения кислорода в крови по ходу капилляра; PAo2 – значение парциального давления кислорода в альвеолярном газе; E ≈ 2,718 – иррациональное число; t – текущее значение времени, сек; T ≈ 0,1 сек – постоянная времени процесса диффузии в легких.
Предполагая, что постоянная времени процесса диффузии в легких при переходе от работы в состоянии покоя к работе в состоянии нагрузки не меняется, используем эту математическую модель для анализа в различных режимах нагрузки.
Настоящее выражение было запрограммировано в среде Microsoft Excel. В результате была получена компьютерная модель диффузии кислорода в легочном капилляре. На данной компьютерной модели были исследованы два режима дыхания: дыхание в состоянии покоя и дыхание при нагрузке мощностью 200 Вт. Результаты исследования получены из модели в виде графика и представлены на рис. 4.
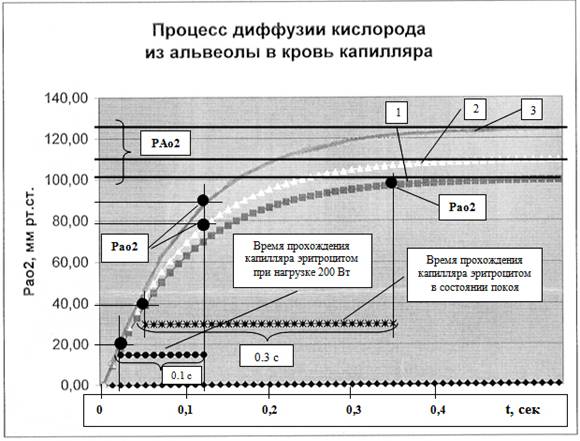
Рис. 4. Результаты математического моделирования процесса диффузии кислорода из альвеолы в кровь легочного капилляра: 1 – процесс изменения Po2 в состоянии покоя; 2 – процесс изменения Po2 при нагрузке 200 Вт без учета динамического давления в альвеолах; 3 – процесс изменения Po2 при нагрузке 200 Вт с учетом динамического давления в альвеолах.
Кривая 1 отражает ход процесса диффузии кислорода из альвеолярного пространства в кровь капилляра в состоянии покоя, описанного в [5].
Как видно из графика, при этих условиях концентрация кислорода в крови на выходе из капилляра близка к 100 мм рт.ст., т.е. эффективность диффузии вполне достаточная.
Кривая 2 отражает ход процесса диффузии кислорода при нагрузке 200 Вт. В этих условиях имеет место повышенная вентиляция, поэтому значение парциального давления кислорода в альвеолярном газе принято равным 110 мм рт.ст. Кроме того, возрастает минутный объем кровообращения до 25 л/мин (в состоянии покоя он принимался равным 5 л/мин). Если учесть, что при нагрузке открываются дополнительно 50% легочных капилляров, то скорость крови в легочном капилляре увеличивается не в 5 раз, а в 3 раза (25/5/1,5=3,33). Следовательно, эритроцит находится в капилляре в течение 0,1 сек.
Кроме того, как видно на рис. 3, кровь входит в капилляр с концентрацией кислорода, соответствующей 20 мм рт.ст. Как показывает график, за время 0,1 сек в этих условиях парциальное давление кислорода в крови успевает подрасти только до 80 мм рт.ст. (аналитический расчет дает 77 мм рт.ст.). На практике же парциальное давление кислорода в артериальной крови достигает более 90 мм рт.ст. Т.е. модель, как и современная наука, не учитывает дополнительного ресурса, используемого дыхательным центром в реальности.
Ввести в модель дополнительный ресурс, значит повысить значение асимптоты. Значение асимптоты для режима нагрузки 200 Вт было повышено настолько, чтобы парциальное давление кислорода в артериальной крови (т.е. на выходе из капилляра) достигло бы 90 мм рт.ст. Этот режим отражает кривая 3. Модель дает значение PAo2=125 мм рт.ст., т.е. на 15 мм рт.ст. больше, чем обеспечивают общепринятые представления о процессе вентиляции легких. Но появление дополнительного ресурса вполне объяснимо, если учесть результаты исследования [2].
Согласно этим исследованиям дыхательная мускулатура обеспечивает не только вентиляцию альвеолярного пространства, но и создает некоторое динамическое давление в альвеолярном пространстве при выдохе. Величина этого давления зависит от аэродинамического сопротивления воздухоносных путей. Аэродинамическое сопротивление, в свою очередь определяется скоростью газового потока, а скорость – частотой дыхания.
Таким образом, обеспечивая необходимую частоту дыхания, дыхательный центр обеспечивает заданную величину концентрации кислорода в артериальной крови. Подтверждают это данные, полученные [4] (см. с. 19, таблица 1). При одной и той же нагрузке (800 кГм/мин) испытуемый дышал либо через нос, либо через рот. При этом при дыхании через рот достоверно возрастала частота дыхания. Но увеличивать вентиляцию легких не было необходимости (значение величины нагрузки сохранялось), поэтому соответственно сокращалась глубина дыхания.
Казалось бы, через рот дышать легче (меньше нагрузка на мускулатуру), вентиляция альвеолярного пространства эффективнее (меньше мертвое пространство, меньше сопротивление воздухоносных путей). Зачем увеличивать частоту дыхания? Ответ обоснован в [2]. Для обеспечения организма кислородом при определенной мощности нагрузки, дыхательный центр создает определенную добавку динамического давления (в нашей модели 15 мм рт.ст.). Но при меньшем аэродинамическом сопротивлении (при дыхании через рот сопротивление меньше, чем при дыхании через нос) для создания того же дополнительного динамического давления требуется большая скорость газового потока. Поэтому дыхательный центр увеличивает частоту дыхания.
Литература
1. Васильев Г.Ф., Кибернетика и биология // Биофизика, 2013, том. 58, вып. 4, с. 732-736
2. Васильев Г.Ф., Динамичное дыхание // Журнал научных публикаций аспирантов и докторантов, Курск. – 2014, - №6, - с. 209-213.
3. Карпман В.Л., Любина Б.Г., Динамика кровообращения у спортсменов. Москва, «Физкультура и спорт», 1982 год.
4. Михайлов В.В. Дыхание спортсмена. Москва, “Физкультура и спорт”, 1983 год.
5. Тевс Г. Легочное дыхание // Физиология человека: в 3-х томах: перевод с англ, под ред. Р. Шмидта и Г. Тевса (Мир, 1996).
6. Doll E. J., Keul J., Maiwald C., Reindell H. «Amer. J. of Physiol» 1968, N1, 215.
Поступила в редакцию 21.11.2014 г.