Физико-химические свойства сплавов системы CuCr2S4-Tl
Абилов Чингиз Ильдырым оглы,
доктор технических наук, профессор,
Азербайджанский технический университет, г. Баку.
Кулиев Адалат Фирудин оглы,
докторант,
Азербайджанский педагогический университет, г. Баку.
Комплексными методами физико-химического анализа впервые построена диаграмма состояния разреза CuCr2S4-Tl, который оказался неквазибинарным сечением в четверной системе Cu-Cr- Tl-S. Выявлено, что характер фазообразования сложный, кристаллизация сплавов завершается в трехфазной смеси, кроме a-твердых растворов на основе CuCr2S4. Таллий, растворяясь в CuCr2S4, образует гомогенную область, граница которой при 300 К доходит до ~5 мол%. Расчетом некоторых термодинамических параметров установлено, что увеличение количества таллия в сплавах, степень диссоциации ослабляется, а вероятность образования сложных ассоциатов усиливается.
Ключевые слова: диаграмма состояния, энергия смещения, энтропия.
В литературе имеются немногочисленные работы по исследованию свойств сплавов (CuCr2S4)1-хTlх, но характер физико-химического взаимодействия и природа фазообразования в системе CuCr2S4-Tl до настоящей времени не изучены. Согласно литературным данным [1] в тройной системе Cu-Tl-S образуется соединение Cu-TlS с температурой конгруэнтного плавления ~689К. Это соединения образуется в разряде CuS-Tl, который, в свою очередь, составляет боковую сторону треугольника CuS - Cr2S3-Tl, в котором находится исследуемый разрез CuCr2S4 -Tl (рис. 1).
Так как соединения CuTlS и Cr2S3 являются конгруэнтно плавящимся соединениями, то квазибинарность разреза CuTlS-Cr2S3 не вызывает сомнения. Соединение же CuCr2S4 – имеет инконгруэнтный характер плавления, отчего и можно ожидать, что разрез CuCr2S4-Tl будет неквазибинарным.
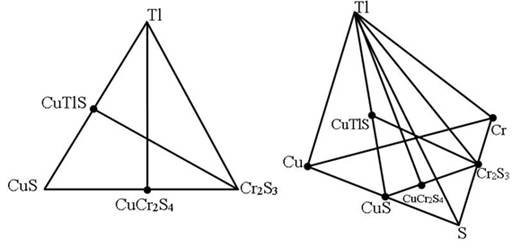
Рис. 1. Разрезы в тройной системе CuS - Tl-Cr2S3 и треугольники в четверной системе Cu-Tl-Cr-S.
Экспериментальная часть
Синтез соединения CuCr2S4 и сплавов системы CuCr2S4- Tl проводили технологией твердофазных реакций из отдельных особо чистых элементов. Реакция образования составляющих компонентов соединения CuCr2S4 происходит в одну стадию при соответствующих температурах; CuS + Cr2 S3 ® CuCr2S4. Результаты проведенного термического анализа, а также учет технологических особенностей, приведенных в [2], предоставили возможность разработать оптимальный вариант синтеза сплавов системы CuCr2S4- Tl.. Вся процедура синтеза и гомогенизации состава (термический отжиг проводили при 1073К в течении 300ч.) имела продолжительность около одного месяца. После гомогенизирующего отжига образцов их приводили в порошковое состояние и прессовали, с дальнейшей выдержкой при 873К в течение одной недели.
Характер физико-химического взаимодействия в системе CuCr2S4-Tl исследовали дифференциально-термическим (ДТА), включая и высокотемпературную (ВДТА), микроструктурным (МСА) и рентгенофазовым (РФА) анализами соответственно на приборах, TERMSKAN-2 и BDTA-8M, MUM-8, D2 FHASER (CuKa излучение с Ni – фильтром). Микротвердость определяли на металлографическом микроскопе ПМТ-3, а плотность измеряли с помощью пикнометра с толуоловой жидкостью.
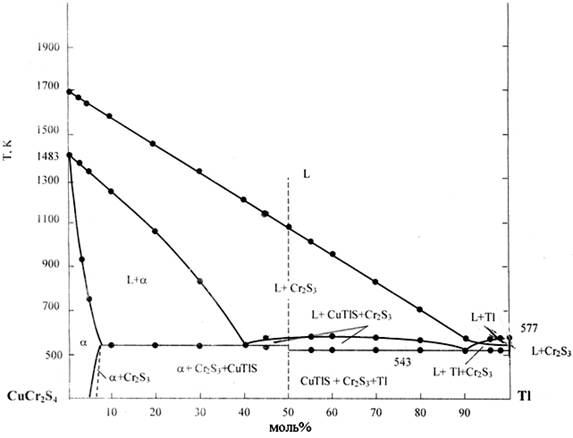
Рис. 2. Диаграмма состояния системы CuCr2S4- Tl.
Результаты экспериментов и их обсуждение
На основе результатов физико-химического анализа построена диаграмма состояния CuCr2S4-Tl (рис. 2). Как видно, система неквазибинарная. На термограммах всех составов (кроме a-твердых растворов и сплавов из области a+ Cr2S3) имеется три экзотермических эффекта. В отличие от системы CuCr2S4-In в этой системе ширина гомогенной области на основе CuCr2S4 узкая и при 300К ее граница доходит до ~95 мол% CuCr2S4 . В этом вопросе немаловажную роль может сыграть размеры атомных радиусов замещающего и замещенных элементов. В системе протекает реакция CuCr2S4 + Tl ® Cu TlS + Cr2S 3 и в результате этого диаграмма состояния системы CuCr2S4-Tl разделяется на две самостоятельные подсистемы. Первичная кристаллизация в обоих подсистемах начинается от Cr2S3. Эвтектика со стороны металлического таллия не вырожденная. Результаты рентгенографического анализа находится в качественном согласии с построенной диаграммой состояния. На рис. 3 приведены рентгенодифрактограммы некоторых составов системы CuCr2S4-Tl .
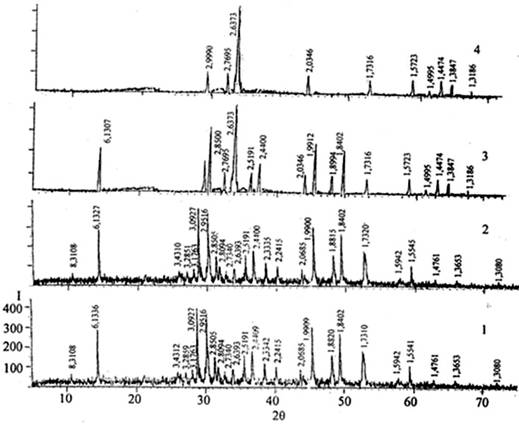
Рис. 3. Рентгенодифрактограммы сплавов системы CuCr2S4-Tl: 1 – CuCr2S4, 2 – 5%Tl, 3 – 40% Tl, 4 – 80% Tl.
Как видно, рентгенограммы CuCr2S4 и 5%Tl мало отличаются. Следовательно, этот состав (95 мол% CuCr2S4) является твердым растворов на основе дихромотетрасульфида меди. Остальные дифрактограммы содержат дифракционные линии чистого CuCr2S4, металлического таллия и промежуточных фаз, образующихся в системе CuCr2S4-Tl
Другие результаты физико-химического анализа, а также составы синтезированных сплавов приведены в табл. 1. Для микротвердости сплавов получены две значения, соответствующих разным составам обогащенных CuCr2S4 и Tl.
Таблица 1.
Составы и некоторые физико-химические свойства сплавов системы CuCr2S4-Tl.
|
N N |
Составы, мол % |
Плотность пикнометрическая, г/см3 |
Микротвердость, МПа |
||
|
Tl |
CuCr2S4 |
Фазы обогащенные в составе Tl (Р=0,05 N) |
Фазы обогащенные в составе CuCr2S4 (Р=0,20 N) |
||
|
1 |
100 |
0 |
11,65 |
150 |
|
|
2 |
95 |
5 |
11,32 |
150 |
|
|
3 |
90 |
10 |
10,94 |
155 |
|
|
4 |
80 |
20 |
10,12 |
160 |
|
|
5 |
70 |
30 |
9,24 |
|
|
|
6 |
60 |
40 |
8,63 |
|
|
|
7 |
50 |
50 |
7,83 |
|
2600 |
|
8 |
40 |
60 |
7,14 |
|
2600 |
|
9 |
30 |
70 |
6,31 |
|
2600 |
|
10 |
20 |
80 |
5,65 |
|
2600 |
|
11 |
10 |
90 |
4,66 |
|
2600 |
|
12 |
5 |
95 |
4,38 |
|
2600 |
|
13 |
0 |
100 |
4,15 |
|
2500 |
Размеры фазы Cr2S3 были маленькими, отчего измерение их микротвердости затруднено.
Для определения степени стабильности образующихся a - твердых растворов рассчитаны некоторые термодинамические параметры сплавов Cu1-х Tlх Cr2S4 (где х £0,2). Один из таких параметров является энергия атомизации (Hs) которую для соединения CuCr2S4 можно записать как:
![]()
Взяв термодинамические
данные для отдельных элементов из [3] и учитывая их в формуле, то получим; ![]() =317,73 кДж/моль.
=317,73 кДж/моль.
Для твердых растворов (CuCr2S4)1-хTlх формула будет имеет вид
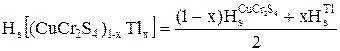
Согласно расчетам получены:
![]()
![]() и
и ![]() .
.
Как видно, переход от соединения CuCr2S4 к твердым растворам (CuCr2S4)1-хTlх с увеличением в составе количества таллия значение энергии атомизации уменьшается, что свидетельствует об ослаблении силы химической связи в твердых растворах, т.е. они являются частично стабильными составами.
Одновременно для сплавов малого замещения Cu1-хTlх Cr2S4 в жидкой фазе рассчитаны значения энергии смещения молекул с допуском энтропии идеальных растворов
![]()
Или же, можно представить, что избыточная энтропия равна нулю. Для неширокой гомогенной области системы CuCr2S4-Tl можно применять приведенной в [4] уравнение смещения энергии в жидкой фазе
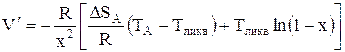 ,
,
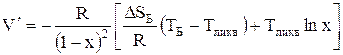 ,
,
где: ![]() - энергия смещения
(Дж/моль),
- энергия смещения
(Дж/моль), ![]() и
и
![]() - энтропия
плавления 1-го и 2-го компонента (Дж/моль∙К), ТА и ТБ
– температуры плавления 1-го и 2-го компонентов (К), х-мольная доля второго
компонента в жидкой фазе, Тликв- температура ликвидуса соответствующего
состава в системе CuCr2S4
– Tl.
- энтропия
плавления 1-го и 2-го компонента (Дж/моль∙К), ТА и ТБ
– температуры плавления 1-го и 2-го компонентов (К), х-мольная доля второго
компонента в жидкой фазе, Тликв- температура ликвидуса соответствующего
состава в системе CuCr2S4
– Tl.
Согласно
нашим расчетам было известно, что ![]() (CuCr2S4) = -15,4
(Дж/моль∙К), а также для таллия ∆Sпл=7,405
Дж/моль∙К и ∆Нпл=267Дж/моль∙К. С учетом Тликв=1705К
для состава х=0,01 получено, что V′=960,203кДж/моль. Рассчитанные значения
энергии межмолекулярного смещения для х=0,03, х=0,05, х=0,1 и х=0,2 в виде
зависимости от состава приведены на рис 4. Как видно, в зависимости от
увеличения количества таллия в составе сплавов значения энергии смещения в
жидкой фазе монотонно уменьшается. Это указывает на слабую диссоциацию взаимодействующих
компонентов, т.е. здесь образование сложных ассоциатов не вызывает сомнения. В
пользу сказанного свидетельствует и характер сложного фазообразования,
изображенного на диаграмме состояния системы CuCr2S4 – Tl.
(CuCr2S4) = -15,4
(Дж/моль∙К), а также для таллия ∆Sпл=7,405
Дж/моль∙К и ∆Нпл=267Дж/моль∙К. С учетом Тликв=1705К
для состава х=0,01 получено, что V′=960,203кДж/моль. Рассчитанные значения
энергии межмолекулярного смещения для х=0,03, х=0,05, х=0,1 и х=0,2 в виде
зависимости от состава приведены на рис 4. Как видно, в зависимости от
увеличения количества таллия в составе сплавов значения энергии смещения в
жидкой фазе монотонно уменьшается. Это указывает на слабую диссоциацию взаимодействующих
компонентов, т.е. здесь образование сложных ассоциатов не вызывает сомнения. В
пользу сказанного свидетельствует и характер сложного фазообразования,
изображенного на диаграмме состояния системы CuCr2S4 – Tl.
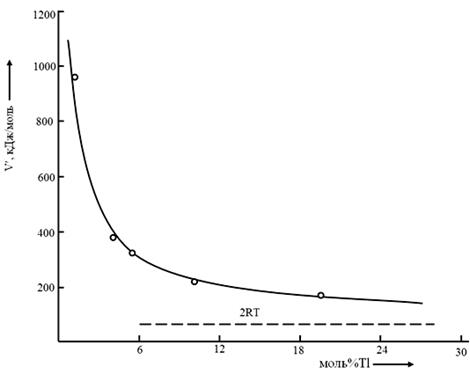
Рис. 4. Зависимость энергии межмолекулярного смещения в жидкой фазе от состава сплавов (CuCr2S4)1-xTl.
Литература
1. Gurdes B., Bruk G., Raymond A., Tedena I.C. Trois phases ternare Cu – Tl – S // Mater.Res.Bull / 19769, Vol.14, №,7, pp.943-946.
2. Аминов Т.Г., Курдянкин Д.И., Шабунина Г.Г., Новоторцев В.М. Синтез и магнитные свойства твердых растворов Cu0,5Fe0,5-xInxCr2S4 // Журнал неорганической химии, 2012, Т.57, №6, с. 853-856.
3. База данных термических констант веществ. Электронная версия. Под.ред.В.С.Юнгмана. 2006, http://www.chem.msu.su/eqibin/tkv.
4. Морачевский А.Г., Сладков Н.Б. Термодинамические расчеты в металлургии. Справочник. М., Металлургия, 1985, 196.
Поступила в редакцию 10.02.2015 г.